Коррозия металла – виды, борьба, методы защиты и предотвращение ржавчины

Что такое коррозия
Коррозия – процесс разрушения металлов под действием химических или электрохимических реакций с окружающей средой с образованием устойчивых соединений (оксидов, гидроксидов, сульфидов). В результате коррозии меняются физические и механические свойства металла:
- Теряется прочность.
- Металл покрывается налётом (ржавчиной).
- Образуются трещины и дырки.
Корродирование металла – сложная цепочка реакций, где одновременно происходят процессы окисления и восстановления. На поверхности образуются участки – аноды и катоды. В анодных зонах металл теряет электроны и превращается в ионы, а в катодных – эти электроны взаимодействуют с кислородом и влагой. Так постепенно накапливаются продукты коррозии, разрушающие поверхность.

Коррозия металла
Причины коррозии
На скорость и характер ржавления металла влияют:
- Влага и кислород. Даже небольшое количество воды на металле способно вызвать ржавчину. В присутствии кислорода начинается окисление – металл теряет электроны, превращаясь в оксиды.
- Солевые и кислотные среды. Соли, особенно хлориды, превращают воду в электролит, ускоряя движение ионов и делая процесс коррозии в десятки раз быстрее. Кислоты также растворяют защитные плёнки и разрушают металл.
- Температура и влажность. Повышение температуры и влажности усиливает химическую активность веществ и ускоряет коррозионные реакции.
- Загрязнения и примеси. Частицы грязи, пыли и масла удерживают влагу и соли на поверхности, тем самым создают благоприятные условия для ржавления.
- Контакт с другими металлами. Во влажной среде разные металлы образуют гальваническую пару – один металл защищается, другой разрушается.
- Механические повреждения и трение. Царапины, сколы и постоянное трение нарушают защитный слой (лак, краску, оксидную плёнку), открывая металл для прямого контакта с влагой и воздухом.
Какие бывают виды коррозии металла
Химическая коррозия
Химическая коррозия происходит без участия электрического тока, напрямую в результате реакции металла с газами или неэлектропроводными жидкостями.
- Протекает при высоких температурах, в сухих газовых средах (в горячем воздухе, парах серы, хлора) и в органических средах, не содержащих воду (масла, топлива, растворители).
- Реакция идёт равномерно по всей поверхности с образованием тонкого слоя оксидов.
- Если оксидная плёнка плотная и прочная, как у алюминия или хрома, она замедляет процесс разрушения и защищает металл от дальнейшего окисления.
- У железа и меди наоборот – продукты коррозии рыхлые и не препятствуют доступу кислорода, поэтому разрушение продолжается.
Электрохимическая коррозия
Электрохимическая коррозия происходит во влажной или жидкой среде, где присутствуют электролиты – растворы солей, кислот или щелочей.
- Поверхность металла разделяется на микрозоны с разным электрическим потенциалом. На аноде металл окисляется и разрушается, а на катоде происходят восстановительные реакции с участием кислорода или водорода. Микротоки от разности потенциалов усиливают разрушение металла.
- Электрохимическая коррозия вызывает появление ржавчины на стальных конструкциях, трубах, автомобилях, подземных кабелях и корпусах судов. Особенно интенсивно развивается в морской воде и влажной почве, где много солей и агрессивных ионов.
Как защитить металл от коррозии
Процесс ржавления металла возможно замедлить или полностью предотвратить, если ограничить контакт металла с агрессивной средой. Основные способы защиты металлов от коррозии:
- Защитные покрытия. Лакокрасочные материалы, порошковая покраска и металлизация формируют плотный слой и изолируют металл от внешней среды.
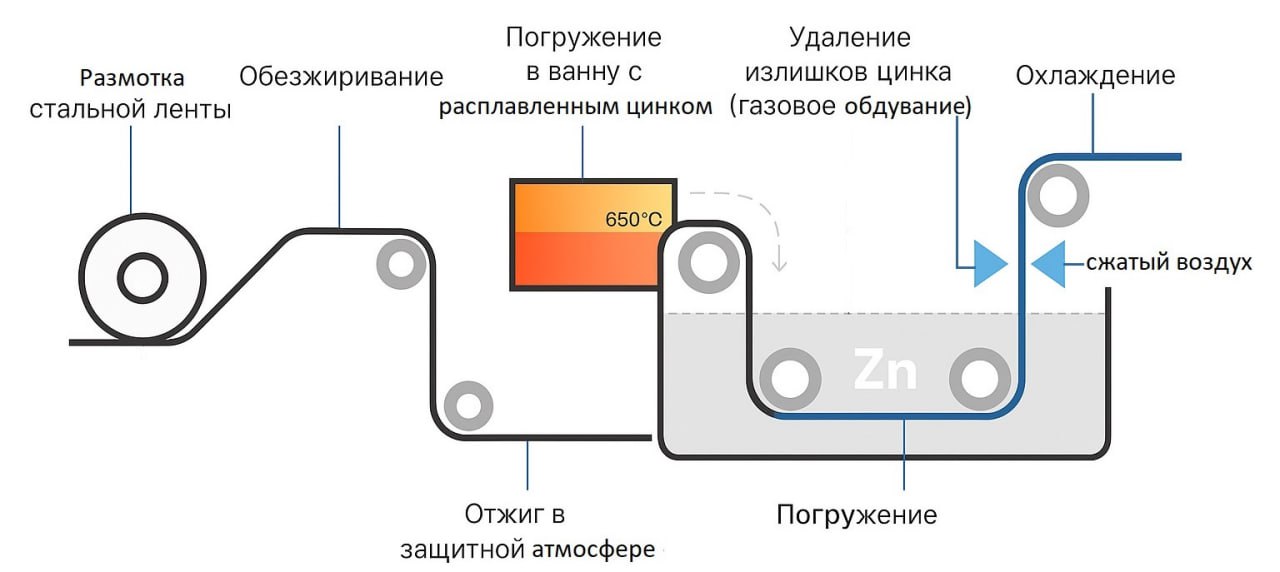
- Цинкование. Металл покрывают слоем цинка методом горячего погружения, холодного цинкования, гальванического осаждения или термодиффузии. Цинк действует как жертвенный анод и первым вступает в реакцию с кислородом и влагой. Даже при повреждении покрытия, цинк продолжает защищать сталь электрохимически.
- Пассивация. Химическая обработка поверхности с образованием тонкой оксидной плёнки. Метод эффективен для нержавеющих сталей и алюминия.
- Легирование. В расплав добавляют хром, никель, молибден, алюминий и другие добавки, которые формируют плотную пассивную плёнку. Так получают нержавеющие стали и жаропрочные сплавы, устойчивые к коррозии во влажной или химически активной среде.
- Катодная и анодная защита. Электрохимический способ, при котором к металлу подключают дополнительный электрод или источник тока. Это смещает потенциал металла и останавливает процесс разрушения.
- Контроль условий эксплуатации. Снижение влажности, защита от прямого контакта с водой и солями, регулярное обслуживание и очистка поверхности продлевают срок службы металла.
Как предотвратить коррозию при прокладке кабеля
Коррозия металлических кабельных лотков и соединительных элементов приводит к ослаблению конструкции, повреждению кабеля и дорогостоящему ремонту. Чтобы избежать корродирования металла, необходимо соблюдать следующие меры при монтаже кабельных систем:
- Использование коррозионно-стойких материалов. Для кабельных проволочных лотков, лестничных лотков, кабельных стоек, кабельных коробов, систем подвеса, креплений, п-профилей металлических, страт профилей и консолей рекомендуется применять оцинкованную сталь, нержавеющую сталь или алюминиевые сплавы.
- Выбор конструкции лотков. Перфорированные кабельные лотки применяют в сухих и проветриваемых помещениях – отверстия обеспечивают вентиляцию и отвод тепла. Неперфорированные (глухие) лотки используют во влажных, пыльных и вредных зонах. В агрессивных средах – лотки для кабеля из нержавеющей стали марок AISI 304 или AISI 316.
- Грамотный монтаж. При установке важно не повреждать защитное покрытие – даже мелкие царапины и сколы могут стать очагами коррозии. Рекомендуется применять качественные крепёжные элементы для лотков и изделия ГЭМ с антикоррозионным покрытием.
- Контроль влажности и вентиляции. В помещениях с повышенной влажностью (подвалы, тоннели, производственные цехи) необходимо предусматривать вентиляцию или дренаж, чтобы исключить скопление конденсата.
- Регулярное обслуживание. Периодический осмотр кабельных трасс, очистка от загрязнений и своевременное восстановление повреждённых участков покрытия предотвращают развитие коррозии.
Типы коррозии материалов
Коррозия развивается по-разному в зависимости от состава металла, условий эксплуатации, наличия электролита и контакта с другими материалами.
- Сплошная коррозия. Охватывает всю поверхность металла. Может быть равномерной, когда разрушение идёт с одинаковой скоростью по всей площади, и неравномерной – процесс развивается с разной интенсивностью на отдельных участках.
- Местная (локальная) коррозия. Поражает отдельные участки поверхности в виде пятен, язв или точечных углублений – питтингов, проникающих в толщу металла.
- Подповерхностная коррозия. Начинается на поверхности, но постепенно развивается в глубине металла. Продукты коррозии скапливаются внутри и вызывают вспучивание и расслоение материала.
- Межкристаллитная коррозия. Разрушение происходит по границам зёрен структуры металла. Внешне изделие выглядит целым, но внутри теряет прочность и пластичность.
- Щелевая коррозия. Возникает в узких зазорах, под прокладками, в резьбовых соединениях и плохо проветриваемых местах. Недостаток кислорода ускоряет процесс разрушения.

Питтинговая коррозия
Какие металлы не ржавеют
Способность сопротивляться коррозии зависит от химического состава металла и способности образовывать на поверхности защитную плёнку, которая изолирует металл от влаги и кислорода.
- Нержавеющая сталь. Содержит не менее 10,5% хрома, который образует прочную оксидную плёнку. Для большей коррозионной стойкости добавляют никель, молибден и титан.
- Алюминий. При контакте с воздухом формируется защитный слой оксидов, который останавливает дальнейшее окисление.
- Цинк. При окислении цинк покрывается плотным слоем карбоната. Этот слой замедляет разрушение металла.
- Медь и её сплавы (латунь, бронза). Медь не ржавеет, но со временем на поверхности появляется зеленоватая плёнка – патина, которая защищает металл от дальнейшего разрушения.
- Титан. На воздухе титан образует оксидную защиту и устойчив даже к морской воде и кислотам.
Чем отличается ржавчина от коррозии
Коррозия – общее понятие, обозначающее разрушение металла под воздействием окружающей среды: влаги, кислорода, химич. веществ или электрических процессов. Степень проявления коррозии определяется составом металла и условиями эксплуатации.
Ржавчина – вид коррозии, характерный для железа и сталей. Ржавчина представляет собой рыхлый буро-красный налёт – оксиды и гидроксиды железа, образующиеся при взаимодействии металла с влагой и кислородом. Ржавчина не защищает металл, как защитная плёнка нержавеющей стали, а ускоряет разрушение.













































.png)